1 Eftergrûn fan 'e dengue-epidemy: In eskalearjende wrâldwide útdaging foar folkssûnens
Dengue is in akute firale sykte dy't troch muggen oerdroegen wurdt, feroarsake troch it denguefirus (DENV), dat wrâldwiid de rapst ferspriede arbovirale sykte is wurden, en in substansjele bedriging foarmet foar de feiligens fan 'e folkssûnens. Yn 'e ôfrûne twa desennia is de wrâldwide ynsidinsje fan dengue dramatysk tanommen, wêrby't it oantal rapportearre gefallen sûnt 2021 jierliks ferdûbele is [1]. Yn desimber 2023 ferklearre de Wrâldsûnensorganisaasje (WHO) in wrâldwide dengue-need om koördinearre ynternasjonale ynspanningen te fersterkjen. Epidemiologyske skattings fan 'e WHO jouwe oan dat sawat 3,9 miljard minsken wrâldwiid risiko hawwe op dengue-ynfeksje, mei nei skatting 390 miljoen ynfeksjes dy't jierliks foarkomme - wêrfan 96 miljoen as klinysk dúdlike gefallen presintearje [1,2].
2 Epidemiologyske hichtepunten
De epidemiologyske skaaimerken fan dengue wurde foarme troch de ynteraksje fan virologyske faktoaren, fektorekology, ymmúnreaksjes fan 'e gasthear en sosjaal-miljeu-omstannichheden. In wiidweidich begryp fan dizze skaaimerken is essensjeel foar de ûntwikkeling fan effektive previnsje- en kontrôlestrategyen, lykas krekte diagnostyske oanpakken.
2.1 Oerdrachtfektoren en stedske oerdrachtpatroanen
Dengue-firus wurdt benammen oerbrocht trochAedes aegypti en Aedes albopictusmuggen. Under dizze vektorsoarten wurdt Aedes aegypti erkend as de meast krityske oerdrachtvektor, karakterisearre troch hege "minslike oanpassingsfermogen" en wiidfersprate fersprieding yn tropyske en subtropyske stedske omjouwings. Oars as oare muggenvektors fan arbovirale patogenen, toant Aedes aegypti de folgjende wichtige epidemiologyske skaaimerken:
-In foarkar foar fokken yn antropogene omjouwings (bygelyks wetteropslachkonteners, fuortsmiten bannen)
-In sterke tropisme foar minsklik bloed as in fiedingsboarne
- Itengedrach oerdeis
Dizze skaaimerken definiearje dengue as in typyske infeksje."stedske ynfeksjesykte",mei in signifikant ferhege oerdrachtseffisjinsje yn tichtbefolke gebieten. Undersyk yn ferbân mei de WHO hat oantoand dat yn stedske omjouwings mei hege tichtheid in ferhege frekwinsje fan kontakt tusken muggen en minsken it basisreproduksjetal (R₀) fan DENV flink ferheegje kin, wêrtroch't de fersprieding fan epidemyen fersnelle wurdt [2].
2.2 Globale ferspriedingstrends en driuwende faktoaren
Neffens rapporten fan 'e WHO is it wrâldwide oantal rapportearre dengue-gefallen de ôfrûne twa desennia eksponentiell tanommen [1,3]. Dizze opwaartse trend wurdt benammen oandreaun troch de folgjende ûnderling ferbûne faktoaren:
(1) Klimaatferoaring: Tanimmende wrâldwide temperatueren wreidzje net allinich it geografyske berik fan geskikte habitats foar muggenfektoren út, mar ferkoartje ek de ekstrinsike ynkubaasjeperioade fan DENV binnen de muggengastheer, wêrtroch't de oerdrachtseffisjinsje ferbettere wurdt. Klimaat-induzearre fariaasjes yn muggentichtens binne troch de WHO validearre as in betroubere foarspeller fan 'e spatiotemporele dynamyk fan dengue-útbraken.
(2) Urbanisaasje: Snelle en net-plande stedsútwreiding hat in oerfloed oan briedgebieten foar muggenfektoren makke, wylst de ferhege befolkingstichtens de kontinuïteit fan DENV-oerdrachtketens fersterke hat.
(3) Wrâldwide befolkingsbeweging: Ynternasjonaal reizgjen en hannel hawwe de rappe grinsferskuiwende oerdracht fan DENV fasilitearre, wêrtroch't de oergong fan ymportearre gefallen nei oanhâldende lokale oerdracht befoardere is. WHO-tafersjochgegevens litte sjen dat tusken 2010 en 2021 de Feriene Steaten 7.528 reisrelatearre dengue-gefallen rapportearre hawwe, wêrfan 3.135 sikehûsopname fereasken en 19 resultearren yn mortaliteit.
(4) Útwreiding fan vektorfersprieding: Wrâldwiid bliuwt it geografyske ferspriedingsgebiet fan Aedes aegypti en Aedes albopictus útwreidzje, wêrby't Aedes-muggen hieltyd mear fêstige wurde yn dielen fan Jeropa. Dêrtroch is dengue evoluearre fan in tradisjoneel regionale epidemy ta in wrâldwide bedriging foar de folkssûnens.
2.3 Mechanismen foar ko-sirkulaasje en reinfeksje fan meardere serotypen
It denguefirus bestiet út fjouwer antigenysk ûnderskate serotypen (DENV-1 oant DENV-4). Ynfeksje mei ien serotype jout langduorjende beskermjende ymmúniteit tsjin dat spesifike serotype, mar allinich tydlike en dielde krúsbeskerming tsjin de oare trije serotypen. De algemiene befolking is universeel gefoelich foar DENV, wêrby't mar in subset fan ynfekteare persoanen klinyske sykte ûntwikkelje [2].
Yn endemyske regio's sirkulearje meardere DENV-serotypen faak tagelyk, wat resulteart yn 'e mooglikheid dat yndividuen yn har libben meardere dengue-ynfeksjes ûnderfine kinne. Epidemiologyske stúdzjes fan 'e WHO hawwe ko-sirkulaasje fan meardere serotypen identifisearre as in wichtige oarsaak fan periodike dengue-útbraken [1].
2.4 Sekundêre ynfeksje en antistof-ôfhinklike ferbettering
In kritysk en unyk ferskynsel yn dengue-epidemiology isantistof-ôfhinklike ferbettering (ADE)Tidens in sekundêre ynfeksje mei in heterolooch DENV-serotype fasilitearje net-neutralisearjende antistoffen dy't produsearre wurde tidens de primêre ynfeksje de yngong fan it firus yn monositen en makrofagen, wêrtroch't de firale replikaasje ferbettere wurdt. Dit meganisme wurdt breed erkend troch de WHO as in wichtige patogene faktor yn slimme dengue, ynklusyf hemorragyske koarts fan dengue en dengue-skoksyndroom [1].
Epidemiologyske gegevens fan 'e WHO litte konsekwint sjen dat persoanen mei in sekundêre dengue-ynfeksje in signifikant heger risiko hawwe op it ûntwikkeljen fan slimme sykte yn ferliking mei dyjingen mei in primêre ynfeksje - in skaaimerk dat fan grut belang is foar syktebewaking en klinysk behear. It is wichtich om te notearjen dat, hoewol it risiko op slimme sykte ferhege is tidens in sekundêre ynfeksje, ynfeksje mei elk DENV-serotype potinsjeel kin ûntwikkelje ta slimme dengue [1].
2.5 Net-spesifike klinyske manifestaasjes en risiko op ferkearde diagnoaze
De klinyske manifestaasjes fan dengue binne opmerklik net-spesifyk, benammen yn 'e iere stadia fan sykte, en oerlappe faak mei dy fan oare troch muggen oerdroegen firale ynfeksjes (bygelyks chikungunya- en Zika-firussen) en ek bepaalde respiratoire ynfeksjes. Skattings fan 'e WHO jouwe oan dat 40-80% fan DENV-ynfeksjes asymptomatysk binne [3].
Typyske klinyske manifestaasjes omfetsje:
-Akute koarts (oanhâldt 2-7 dagen, kin twa kear sa faak foarkomme)
-Slimme hoofdpijn en retro-orbitale pine (pine efter de eagen)
-Spier- en gewrichtspine (meastal oantsjutten as "brekbonkekoarts")
-Makulêre of makulopapulêre útslach
- Milde hemorragyske manifestaasjes (bygelyks ekchymose, epistaxis, gingivale bloeding)
Symptomatyske dengue wurdt typysk ferdield yn trije ûnderskate fazen: de koartsfaze, de krityske faze en de herstelfaze. Ungefear minder as 5% fan symptomatyske pasjinten ûntwikkelje ta slimme dengue. Troch it ûntbrekken fan spesifike klinyske skaaimerken is diagnoaze allinich basearre op klinyske symptomen lestich, wat it risiko op ferkearde diagnoaze en ûnderdiagnoaze fergruttet. De WHO beklammet eksplisyt dat klinyske diagnoaze allinich net genôch is om krektens te garandearjen, wêrtroch laboratoariumbefêstiging ûnmisber is [1].
3 wichtige punten fan 'e WHO "Laboratoariumtests foar denguefirus: tydlike rjochtlinen, april 2025"
Yn april 2025 hat de Wrâldsûnensorganisaasje bywurke tydlike rjochtlinen oer laboratoariumtests foar DENV útbrocht, mei autoritative technyske rjochtlinen foar wrâldwide dengue-diagnoaze. Dizze rjochtlinen synthetisearje it lêste bewiis oer dengue-laboratoariumtests yn 'e kontekst fan' e oanhâldende wrâldwide dengue-need en biede praktyske oanbefellings oanpast oan omjouwings mei ferskillende nivo's fan boarnen.

3.1 Fundamentele prinsipes fan teststrategy
De rjochtlinen beklamje dat by de diagnoaze fan dengue in kombineare teststrategy mei meardere markers moat wurde brûkt, basearre op it stadium fan 'e sykte [1]. Mei it each op it ûntbrekken fan in universeel diagnostysk algoritme moatte teststrategyen oanpast wurde oan lokale epidemiologyske konteksten, wêrby't rekken holden wurdt mei de folgjende wichtige faktoaren [1]:
-Ynfeksjestadium: It oantal dagen nei it begjin fan it symptoom bepaalt de meast geskikte testmetoade
-Monstertype: De geskiktheid fan folslein bloed, plasma of serum foar DENV-deteksje
-Regionale epidemiology: De lokaal sirkulearjende DENV-serotypen en ko-sirkulaasje fan oare arbovirussen
-Risiko fan ko-ynfeksje: Yn regio's mei oerlappende arbovirussirkulaasje moat multiplex-testen wurde beskôge om ûnderskied te meitsjen tusken ferskate patogenen
3.2 Teststrategy op basis fan stadia
Neffens de rjochtlinen fan 'e WHO moatte dengue-laboratoariumtests dúdlike tiidsfinsters folgje basearre op it stadium fan 'e sykte [1,2]:
(1) Akute-faze-testen (≤7 dagen nei it begjin)
-Nukleinezuurtesten (Molekulêre testen): Reverse transkripsje-polymerasekettingreaksje (RT-PCR) en oare molekulêre metoaden detektearje DENV RNA mei hege gefoelichheid.
-Antigeentesten: NS1-antigendeteksje, dy't binnen 1-3 dagen nei it begjin detektearber wurdt.
Tidens de akute faze binne de viremienivo's relatyf heech, en berikke nukleïnezuur- en antygentesten optimale gefoelichheid.
(2) Testen yn 'e herstelfaze (≥4 dagen nei it begjin)
-Serologyske testen: IgM-antistoffen wurde typysk om dei 4 nei it begjin detektearber.
-Yn 'e measte gefallen bliuwe IgM-antistoffen 14-20 dagen oanhâlden, en yn guon gefallen kin it oant 90 dagen oanhâlde.
-IgG-testen hawwe beheinde wearde foar de diagnoaze fan akute dengue fanwegen potinsjele krúsreaktive antistoffen fan eardere flavivirus-ynfeksje of faksinaasje.
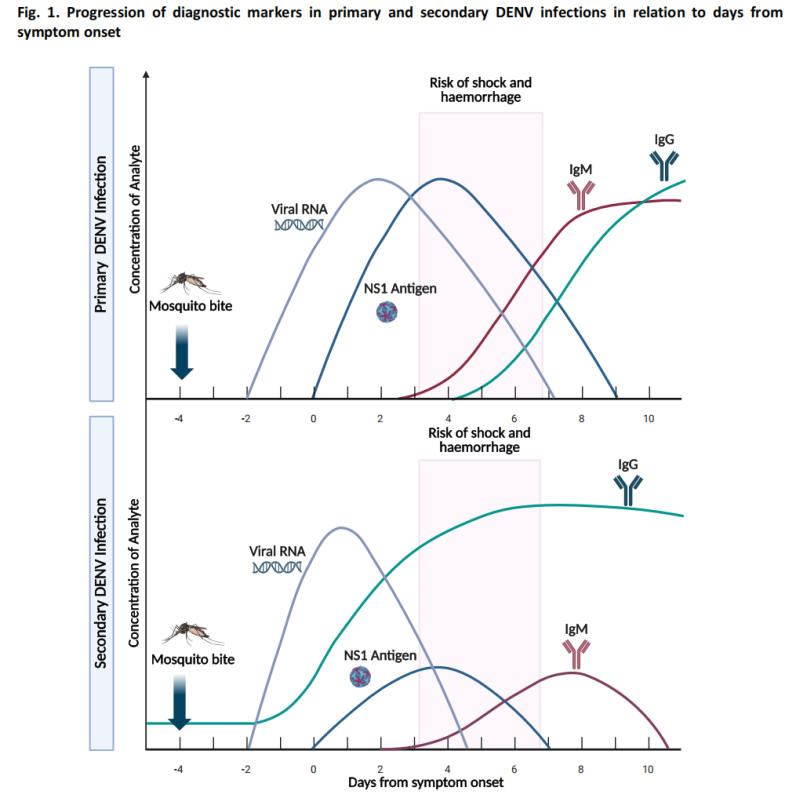
(3) Algoritme foar fertochte gefallendiagnostyk
De rjochtlinen omfetsje in diagnostysk algoritme foar fertochte dengue-gefallen, en riede passende testmetoaden oan op basis fan dagen nei it begjin fan it symptoom: NS1-antigentesten en nukleïnezuurtesten binne de primêre oanpakken yn 'e iere faze, wylst serologyske testen de primêre metoade is yn 'e lettere faze.
3.3 Evaluaasje en seleksje fan testmetoadeprestaasjes
Neffens de WHO is in systematyske evaluaasje fan 'e prestaasjes en tapasbere senario's fan ferskate dengue-testen as folget:
| Testmetoade | Doel | Tiidfinster | Primêr applikaasjescenario | Oerwagings |
| Nukleïnezuurtesten | Firale RNA | 1-7 dagen nei it begjin | Iere befêstiging, serotype-identifikaasje | Gouden standertmetoade; fereasket spesjalisearre laboratoariumapparatuer en technyske ekspertize |
| NS1 Antigentesten | Net-struktureel proteïne | 1-3 dagen nei it begjin | Iere rappe screening | Beskikber yn rappe diagnostyske test (RDT) formaat, geskikt foar ynstellings mei beheinde boarnen |
| IgM-antistoftesten | Spesifike IgM-antistoffen | ≥4 dagen nei it begjin | Diagnoaze fan resinte ynfeksje | In inkele serummonster suggerearret allinich in mooglike resinte ynfeksje; serokonverzje is fereaske foar befêstiging |
| IgG-antistoftesten | Spesifike IgG-antistoffen | Herstellende/eardere ynfeksje | Epidemiologysk ûndersyk, beoardieling fan immuniteitsstatus | In inkele serummonster is net geskikt foar akute dengue-diagnoaze |
| Kombineare testen (NS1+IgM/IgG) | Antigeen + Antistoffen | Folsleine sykteferrin | Wiidweidige diagnoaze fan dengue-ynfeksje | Op it stuit it bêst prestearjende RDT-formaat foar dengue-diagnoaze |
| NGS | Firale RNA | 1-7 dagen nei it begjin | Virale genomyske tafersjoch | Fereasket spesjalisearre sekwinsjeapparatuer en bioinformatyske analysemooglikheden |
4 Oanbefellings foar makro- en mikrotest-produkten foar denguedeteksje per senario
Om dengueprevinsje en -bestriding te stypjen, biedt Macro & Micro-Test in yntegreare diagnostykportfolio dy't rappe screening, molekulêre befêstiging en genomyske tafersjoch omfettet, en foldocht oan behoeften yn ferskate stadia fan útbraakbehear.
4.1 Senario 1: Fluchscreening en rjochte tafersjoch
Fan tapassing op koartskliniken, primêre sûnenssoarchfoarsjennings, screening yn 'e mienskip foar útbraken, en haven-/grinskarantêne.
-Dengue Virus NS1 Antigen Rapid Test: Detektearret iere ynfeksje (1-3 dagen nei it begjin) mei resultaten binnen 15 minuten foar rappe triage.
-Denguevirus IgM/IgG-antistoftest: ûnderskiedt primêre/sekundêre ynfeksjes om it risiko op swiere sykte te evaluearjen.
-Dengue Virus NS1 Antigen + IgM/IgG Kombineare Rapid Test: Detektearret tagelyk antigen en antistoffen foar in folsleine diagnoaze.
-Chikungunya-firus IgM/IgG-antistoftest: Maakt differinsjaaldiagnoaze mei dengue mooglik om patogenen sekuer te identifisearjen.
4.2 Senario 2: Presyzjediagnoaze en needreaksje
-Denguevirus I/II/III/IV Nukleïnezuurdeteksjekit: Detekteart en ûnderskiedt 4 serotypen (deteksjelimyt 500 kopyen/mL) foar it opspoaren fan útbraken.
-Lyofilisearre Dengue-firus PCR-kit: ferfierber op keamertemperatuer, geskikt foar gebieten mei beheinde boarnen en hommelse útbraken.
-Dengue/Zika/Chikungunya Multiplex Real-Time PCR Kit: Detekteart tagelyk 3 arbovirussen foar effisjinte differinsjaaldiagnoaze by komplekse útbraken.

Alle boppesteande reagentia binne kompatibel mei it AIO 800 folslein automatisearre sample-nei-antwurdsysteem, wêrtroch't hânmjittige operaasje en krúsbesmetting wurde fermindere, en de effisjinsje en biofeiligens wurde ferbettere.
4.3 Senario 3: Genomysk tafersjoch en firale lineage-analyze
Fan tapassing op nasjonale referinsjelaboratoria, ûndersyksynstellingen foar folkssûnens, yn oerienstimming mei de posysje fan 'e WHO fan NGS.
De genomyske tafersjochoplossingen fan Macro & Micro-Test stypje it sekwinsjearjen fan it hiele genoom foar it tracearjen fan firussen, ferdúdliking fan 'e oerdrachtketen, monitoring fan farianten en oanpassing fan faksinstrategyen. Se stypje manuele/automatisearre workflows, ferbetterje de trochfier en reprodusearberens, wêrtroch laboratoaria kinne opwurdearje fan routinetests nei avansearre tafersjoch, yn oerienstimming mei de klam fan 'e WHO op it fersterkjen fan it monitoring fan firale evolúsje.

4.4 Wearde fan yntegreare oplossingen
Macro & Micro-Test biedt folsleine diagnostyske oplossingen foar it opspoaren fan arbovirussen, en stipet elke faze fan útbraakbehear: rappe screeningtools foar sûnenssoarchynstellingen oan 'e frontline, molekulêre befêstiging foar presyzjediagnoaze, en mooglikheden foar it analysearjen fan it heule genoom foar epidemiologysk tafersjoch. Mei hege prestaasjes assays, fleksibele workflows en automatisearringsklare platfoarms, jouwe dizze oplossingen laboratoaria en folkssûnenssystemen de mooglikheid om de tarieding en reaksje op opkommende arbovirusbedrigingen wrâldwiid te fersterkjen.
Referinsjes
[1] Wrâldsûnensorganisaasje. Laboratoariumtests foar denguefirus: tydlike rjochtlinen, april 2025. Genève: Wrâldsûnensorganisaasje; 2025.
[2] WHO Global Arbovirus Initiative Technical Advisory Group. Fersterking fan wrâldwide tarieding en reaksje op bedrigingen fan arbovirale sykten: In oprop ta aksje. Lancet Infect Dis. 2026;26(1):15-17.
[3] De Lancet-mikrobe. It oerwinnen fan it dilemma fan dengue-diagnostyk. Lancet-mikrobe. 2025;6(7):101190.
Pleatsingstiid: 20 maart 2026
